O RYR1 é um dos maiores genes do corpo humano, e é responsável para o funcionamento dos nossos músculos.
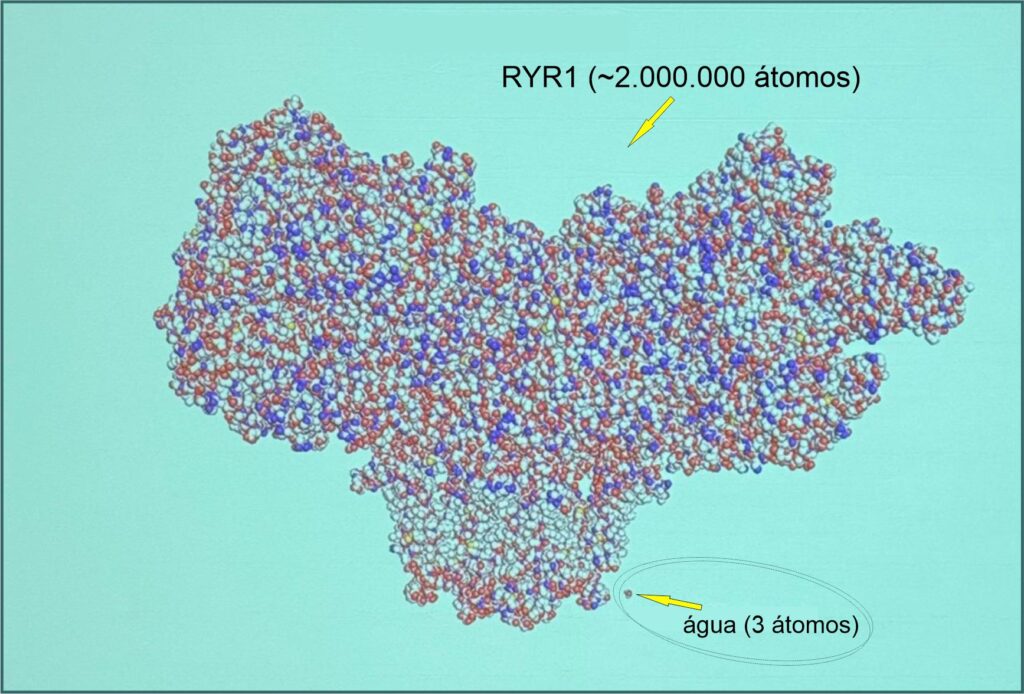
O gene RYR1 (Receptor de Rianodina 1) é um dos maiores e mais complexos genes do genoma humano. Ele contém mais de 100 exons e cerca de 15 mil pares de bases na sua sequencia de DNA, abrangendo uma grande extensão no cromossomo 19. A estimativa é que o gene RYR1 tenha cerca de 2 milhões de átomos, e esse é somente um cálculo de aproximação, pois a quantidade exata pode variar dependendo da sequência específica de nucleotídeos.
Para se ter uma idéia da complexidade do RYR1, ele é imensamente maior e mais complexo do que moléculas simples como da água, tão crucial para nossa vida, e a título de comparação, pasmem ! …o RYR1 tem 2 milhões de átomos, e a água, também conhecida como H20, tem somente 3 átomos.
O gene RYR1 que é crucial para a função do receptor de rianodina, que é um canal de cálcio localizado no Retículo 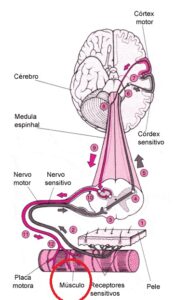 Sarcoplasmático (RS) das células musculares esqueléticas, e desempenha um papel importante no controle de liberação de íons de cálcio para dentro das células musculares, essencial no mecanismo de funcionamento do músculo, especificamente fundamental para o Acoplamento Excitação-Contração (AEC), processo de contração e relaxamento muscular. O processo funciona assim: 1). O sinal nervoso (potencial de ação) atinge o receptor DHPR na membrana da célula; 2). O DHPR, que está ligado mecanicamente ao RYR1, ele é acionado e abre o canal RYR1; 3). O RYR1 aberto libera grandes quantidades de cálcio (Ca2+
Sarcoplasmático (RS) das células musculares esqueléticas, e desempenha um papel importante no controle de liberação de íons de cálcio para dentro das células musculares, essencial no mecanismo de funcionamento do músculo, especificamente fundamental para o Acoplamento Excitação-Contração (AEC), processo de contração e relaxamento muscular. O processo funciona assim: 1). O sinal nervoso (potencial de ação) atinge o receptor DHPR na membrana da célula; 2). O DHPR, que está ligado mecanicamente ao RYR1, ele é acionado e abre o canal RYR1; 3). O RYR1 aberto libera grandes quantidades de cálcio (Ca2+) do RS para o citoplasma; 4). O cálcio dispara a contração muscular ao permitir a interação Actina-Miosina; 5). Para o relaxamento, o sinal cessa, o RYR1 se fecha, e rapidamente retorna o cálcio do citoplasma, devolvendo-o ao RS.
Em resumo, o RYR1 atua como o principal portão de saída do cálcio do reservatório intracelular. Ele é o mediador essencial que garante que o comando elétrico do nervo seja traduzido em movimento mecânico, controlando a entrada abrupta de cálcio que inicia a contração e, consequentemente, permitindo que a sua reabsorção finalize o processo para o relaxamento.
Como disse no início deste texto, devido ao tamanho e complexidade do RYR1, mutações nesse gene podem estar associadas a várias doenças musculares, incluindo:
O estudo científico do RYR1 é importante para entender essas condições ou doenças, e desenvolver tratamentos adequados em busca de minimizar seus efeitos e sintomas, pensando até na sua própria cura. Além disso, a análise genética pode ajudar em diagnósticos precoces e na prevenção de complicações associadas a essas doenças.
Durante o tempo que tenho acompanhado a movimentação de informações em torno das questões relacionadas ao RYR1, observo um grande esforço da comunidade científica em busca de entender o mecanismo de funcionamento deste complexo e grandioso gene, grande no tamanho, mas sobretudo grande em sua importância. Essas questões fazem com que o desafio ainda seja maior não só por conta dos indivíduos que têm uma doença a ele relacionada, mas também para compreensão sobre o impacto do envelhecimento celular em qualquer outro indivíduo. Observo também um grande movimento de trabalhos sendo desenvolvidos por cientistas de toda parte do mundo em busca de desenvolver uma droga para tratamentos adequados, para de repente ao menos minimizar seus efeitos e sintomas, até sua cura das doenças relacionadas ao RYR1. Particularmente, minha percepção é que as pesquisas através da técnica de reposicionamento de drogas, também chamado de redirecionamento de fármacos têm se mostrado mais promissoras no curto prazo. O “reposicionamento de drogas” se trata de uma estratégia que busca descobrir novas aplicações terapêuticas para medicamentos já existentes, que originalmente foram desenvolvidos para tratar outras doenças. Essa técnica tem a vantagem por seus reduzidos custos, assim como pela redução de tempo gasto no processo de desenvolvimento, e menores riscos no uso da eventual droga, pois já se conhece a farmacocinética e toxicidade do medicamento pesquisado, um exemplo real e prático de pesquisa em curso está se dando com o Sulfato de Salbutamol.
Contudo, a terapia genética também tem se mostrado uma abordagem promissora para o tratamento e cura de diversas doenças genéticas, oferecendo a possibilidade de corrigir ou substituir genes defeituosos. Embora este tipo de tratamento ainda esteja em desenvolvimento e não seja uma solução universal para algumas doenças, como por exemplo certas formas de miopatias ou doenças hereditárias, os resultados das pesquisas têm sido encorajadores. No entanto, a eficácia e a segurança da terapia genética podem variar dependendo da doença, do tipo de terapia utilizada, e condições do paciente. Além disso, questões éticas e de custo também são consideradas importantes. Contudo, enquanto a terapia genética oferece uma expectativa otimista, é uma área em evolução que requer mais pesquisas, altos recursos financeiros, e testes clínicos para se consolidar como a melhor solução para todas as doenças genéticas.
No caso específico das doenças relacionadas à mutação do gene RYR1, a terapia genética apresenta vários desafios, principalmente, como escrito no início deste texto, devido ao tamanho do gene, complexidade das doenças relacionadas a ele, mas também por considerar que os músculos representam aproximadamente 40% da massa total do corpo humano, e a maior parte dessa massa muscular é composta por músculos esqueléticos. Observe a seguir algumas das dificuldades:
Esses desafios tornam a pesquisa e o desenvolvimento de terapias para mutações no gene RYR1 complexos e exigem abordagens inovadoras e multidisciplinares.
Eu, enquanto portador de uma doença causada pela mutação nesse “grandioso” RYR1, tenho uma relação muito particular com esse gene, e a cada dia que passa o conheço um pouco mais, ..... confira minha próxima postagem intitulada “Eu vi o meu gene em 3D e entendi o que acontece dentro de mim”.
Recentemente foi publicado um artigo médico-científico tratando sobre a Pancreatite em Indivíduos com Doenças Relacionadas ao RYR1. O estudo teve participação de pesquisadores do Reino Unido, Holanda e Estados Unidos, além do nobre apoio da Fundação RYR1.
Mutações no gene do receptor de rianodina do músculo esquelético (RYR1) são uma causa comum de doenças neuromusculares hereditárias e têm sido associadas a um amplo espectro de fenotípico, variando de várias miopatias congênitas de início precoce com fraqueza muitas vezes substancial, até fenótipos induzidos em indivíduos “normalmente fortes” tais como a Rabdomiólise por Esforço (ERM) e suscetibilidade aos efeitos relacionados à anestesia, como a Hipertermia Maligna (HM). O gene RYR1 codifica o principal canal de liberação de cálcio do retículo sarcoplasmático (SR) com um papel crucial
no acoplamento excitação-contração (ECC), processo pelo qual um impulso neuronal elétrico é traduzido em contração muscular por meio da liberação de cálcio intracelular, estimulando o filamento contrátil. Mutações no gene RYR1 associadas à fraqueza muscular permanente normalmente prejudicam o processo excitação-contração (ECC) de forma eficaz, enquanto aquelas associadas com ERM e MH resultam em um receptor RYR1 hiperexcitável e muitas vezes aumenta desproporcionalmente a liberação de cálcio.
Os genes RYR1s foram implicados em processos essenciais de sinalização de cálcio em uma ampla gama de tecidos, mas as manifestações de doenças humanas associadas ao mau funcionamento do RYR1 em outros órgãos além do músculo esquelético até agora receberam pouca atenção. Descobriu-se que os genes RYR1s são amplamente expressos no pâncreas de mamíferos, através de seu papel nos processos de sinalização de cálcio intracelular, e têm sido criticamente implicados na função pancreática endócrina e exócrina.
No estudo foi relatado três casos com características principais de um distúrbio relacionado ao RYR1 e uma história adicional de pancreatite (aguda) inexplicável, sugerindo uma nova associação clínica de função perturbada do RYR1 não relacionada ao músculo estriado. Os três pacientes com diagnóstico de Miopatia Central Core (CCD), Síndrome de King-Denborough (KDS) e Suscetibilidade à Hipertermia Maligna (MHS), respectivamente, que além de seu (suposto) distúrbio relacionado ao RYR1 também desenvolveram sintomas e sinais de pancreatite aguda. Em dois pacientes, os episódios foram recorrentes, com grave envolvimento multissistêmico e sequelas. A sinalização de cálcio mediada por RYR1 desempenha um papel importante na função pancreática normal, mas também tem sido criticamente implicada na fisiopatologia da pancreatite aguda, particularmente nas formas induzidas por ácidos biliares e etanol. Os resultados de modelos animais relevantes indicam que os danos pancreáticos nestas condições podem ser melhorados através da administração do antagonista específico de RYR1, dantroleno, e de outros compostos que modificam o metabolismo pancreático, incluindo a sinalização de cálcio. Estas observações sugerem que os pacientes com variantes de ganho de função do RYR1 podem ter um risco aumentado de desenvolver pancreatite aguda, uma condição que deve, portanto, ser considerada na vigilância da saúde desses indivíduos.
Saiba mais detalhes sobre o tema
deste texto lendo a publicação
completa no artigo científico
clicando na imagem ao lado ⇒
A terapia genética que era tida como uma futura grande promessa para o tratamento de miopatias relacionadas ao RYR1, se torna uma realidade com a publicação do recente relato científico da primeira correção por Edição Prime de uma mutação no gene RYR1.
A Fundação RYR-1 (https://ryr1.org/) cumprimentou a todos no início de ano com um “Feliz 2024, mas também compartilhou a informação que financiou uma pesquisa incrivelmente importante com o Dr. Jacques P. Tremblay, um pesquisador na Universidade Laval em Quebec. As descobertas e resultados dos trabalhos de pesquisa acabaram de ser publicadas em um novo artigo de  pesquisa (https://www.mdpi.com/2073-4409/13/1/31#). E o resultado é ainda mais emocionante, pois os pesquisadores utilizaram com sucesso a Edição Prime, uma forma de edição genética, que foi utilizada para corrigir uma mutação no gene RYR1 nas células musculares esqueléticas. Esta pesquisa fornece "prova de conceito" para a edição de genes como sendo uma estratégia em potencial para tratar miopatias relacionadas com RYR-1, que atualmente carecem de terapias eficazes. Segundo o cientista, "estes resultados são as primeiras demonstrações de que é possível corrigir mutações no gene RYR-1"
pesquisa (https://www.mdpi.com/2073-4409/13/1/31#). E o resultado é ainda mais emocionante, pois os pesquisadores utilizaram com sucesso a Edição Prime, uma forma de edição genética, que foi utilizada para corrigir uma mutação no gene RYR1 nas células musculares esqueléticas. Esta pesquisa fornece "prova de conceito" para a edição de genes como sendo uma estratégia em potencial para tratar miopatias relacionadas com RYR-1, que atualmente carecem de terapias eficazes. Segundo o cientista, "estes resultados são as primeiras demonstrações de que é possível corrigir mutações no gene RYR-1"
O gene RYR1 codifica um canal de cálcio denominado receptor 1 de Ryanodina, apresentada nas fibras musculares esqueléticas. A falha desse canal causa fraqueza muscular, que degenera acarretando deficiências motoras no indivíduo afetado. Atualmente, não existem tratamentos eficazes para estas miopatias, também conhecidas como doenças relacionadas ao RYR1, que são causadas principalmente por mutações pontuais. A Edição Prime permite a modificação precisa de nucleotídeos no DNA. Os resultados dos trabalhos de pesquisa pelos cientistas Kelly Godbout, Joël Rousseau e Jacques P. Tremblay, demostraram uma taxa de correção de 59% da mutação T4709M no gene RYR1 em mioblastos humanos pela entrega de RNA dos componentes de Edição Prime. Deve-se notar que o T4709M é recessivo e, portanto, as pessoas com mutação heterozigótica são saudáveis. Estes resultados são a primeira demonstração de que é possível corrigir mutações no gene RYR1.
A tecnologia de Edição Prime pode ser usada para corrigir mutações que causam miopatias relacionadas ao RYR1. Este grupo de doenças inclui a Hipertermia Maligna (HM), Miopatia Central Core (CCD), Miopaty Multi-Minicore (MmD), Miopatia Centronuclear (CNM), Desproporção Congênita do Tipo de Fibra (CFTD) e Rabdomiólise por Esforço (ERM). Até o momento, mais de 700 variantes no gene RYR1 foram identificadas. Este gene que codifica uma proteína chamada "receptor de rianodina 1" (RyR1), é o principal canal de cálcio no retículo sarcoplasmático (SR) nas fibras musculares esqueléticas. A disfunção desta proteína afeta o fluxo de cálcio para os músculos. A posição da mutação não afetará ou impactará na proteína, mas as mutações nos genes farão com que ocorra principalmente a um vazamento de cálcio. E como o cálcio é fundamental para a contração muscular, essa desregulação do RYR1 leva à fraqueza muscular, caibras, exaustão, intolerância ao calor, dificuldades respiratórias e até mesmo à reação maligna de hipertermia, ou Hipertermia Maligna. Essas miopatias, portanto, afetam gravemente a qualidade de vida dos pacientes. A proteína RYR1 tem variações funcionais limitadas, e o gene RYR1 é um dos mais intolerantes a variações de sequência no genoma humano.
Até o momento, não existe tratamento eficaz para essas doenças relacionadas ao RYR1. Como muitas mutações nos genes RYR1 são mutações pontuais, os resultados descritos no referido artigo demonstram claramente que a Edição Prime pode ser utilizada para corrigi-las, uma vez que pode substituir qualquer nucleotídeo do genoma.
O referido artigo relata a correção de uma dessas mutações (isto é, a T4709M) como exemplo. Esta mutação específica foi selecionada porque existe um modelo de camundongo (RYR1TM/Indel) com essa mutação que desenvolve sintomas claros. Confira o artigo científico no link -> https://www.mdpi.com/2073-4409/13/1/31#
TERAPIA GENÉTICA
A terapia genética é uma grande promessa para o tratamento de doenças genéticas, uma vez que aborda diretamente a raiz do problema. Ao corrigir mutações, a terapia genética tem o potencial de curar milhares de doenças hereditárias.
A descoberta do CRISPR/Cas9 em 2012 foi um marco no desenvolvimento de terapias genéticas. O Crispr/Cas9 é uma espécie de "tesoura genética", que permite à ciência mudar parte do código genético de uma célula. Com essa "tesoura", é possível, por exemplo, "cortar" uma parte específica do DNA, fazendo com que a célula produza ou não determinadas proteínas.
Este sistema usa uma nuclease Cas9 que induz uma quebra da fita dupla do DNA em um local preciso do genoma. Cas9 é direcionado para a sequência do genoma desejada por um único RNA guia (sgRNA). Este sgRNA é um RNA de fita simples complementar a uma sequência de DNA. A proteína Cas9 forma um complexo com o sgRNA e se liga a um motivo adjacente no DNA, induzindo um corte. Após a quebra da cadeia dupla no local do desejado, a célula irá reparar este corte por Reparação Dirigida por Homologia (HDR) se for fornecida uma sequência doadora. No entanto, a percentagem de correção de uma mutação precisa de nucleótidos por HDR é demasiado baixa para ser utilizada no tratamento de doenças hereditárias in vivo . Se nenhuma sequência doadora for fornecida, a célula reparará o corte por junção final não homóloga (NHEJ) e produzirá indels. InDels (inserções e deleções) são adições ou perdas de uma ou mais bases consecutivas na sequência do DNA.
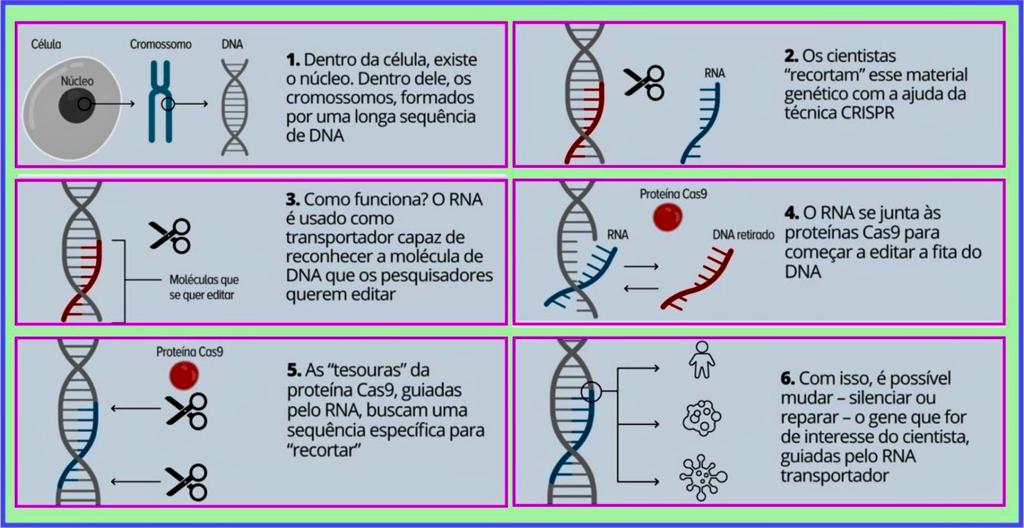
CRISPR/Cas9
Em outubro de 2019, o grupo de David R. Liu publicou uma técnica notável chamada PRIME EDITION. Este sistema pode realizar inserções, deleções direcionadas e todas as 12 conversões de base possíveis.
O Prime Edition ou sistema Edição Prime (em português), é um método de edição de genoma que grava diretamente novas informações genéticas em um local (endereço) de DNA especificado usando uma endonuclease Cas9 prejudicada cataliticamente e fundida com uma transcriptase reversa projetada, programada com um RNA de guia Prime Edition (pegRNA) que especifica o local de destino e codifica a edição desejada. Esta tecnologia realiza modificações no DNA com precisão sem precedentes e oferece vantagens substanciais sobre o sistema tradicional CRISPR/Cas9.
Prime Editing é mais complexo que a edição CRISPR. Ele pode excluir comprimentos longos de DNA causador de doença ou inserir DNA para reparar mutações perigosas, tudo sem desencadear as respostas caóticas (e possivelmente prejudiciais) do genoma introduzidas por outras formas de CRISPR.
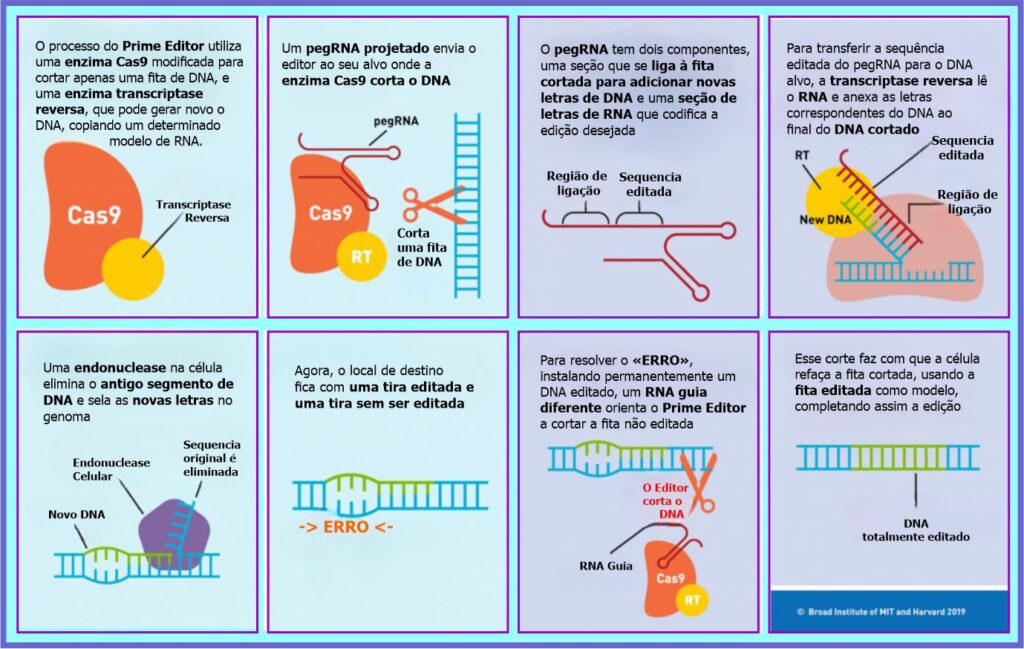
Prime Edition
Em resumo, a técnica CRISPR-Cas9, popularmente utilizada para modificação genética pela comunidade científica, baseia-se na atividade nuclease da enzima Cas9 que corta as duas fitas de DNA, e utiliza a maquinaria de reparo de danos da própria célula. No entanto, o sistema de reparo pode inserir ou deletar letras de DNA, causando efeitos inesperados. Já a nova tecnologia “Prime Editing” ou Edição Prime utiliza uma versão enzima Cas9 que além de reconhecer sequências específicas de DNA, corta apenas uma das fitas da dupla-hélice. Dessa forma, a edição ocorre no local correto do corte através da ação de uma enzima transcriptase e uma fita de RNA guia (pegRNA).
O diagnóstico de uma doença rara impõe ao indivíduo afetado além das consequências físicas a ela inerentes, alterações na sua rotina de vida. Esse mesmo diagnóstico pode pôr fim a um período de vida marcado por incertezas e ansiedades, muitas vezes em razão de uma demorada e sofrida peregrinação por consultas e exames médicos. Entretanto, com o diagnóstico em mãos começa-se uma nova etapa, que é a busca por respostas acerca da doença em questão, e que muitas vezes o médico não conseguiu responder. E o maior desafio em meio a essas buscas se dá por um tratamento eficiente visando a cura, ou ao menos de um que seja pelo alívio do seu sofrimento físico. Portanto, para o paciente essa dura realidade do diagnóstico, é normalmente dividida em duas etapas, uma que acontece no consultório médico, e a outra etapa, que se vive dentro das "quatro paredes da sua intimidade". O processo de assimilação do diagnóstico pode ser assustador e cheio de interrogações, e o indivíduo afetado tende buscar por si só as respostas que mais anseiam, tais como sobre prognóstico, cura, e tratamento. Essas buscas e pesquisas são normalmente feitas na internet, contudo, muitas vezes ao contrário de esclarecer a situação, pode torná-la mais confusa.
Entendo perfeitamente a reação desses indivíduos afetados, assim como de seus familiares, uma vez que o desconhecimento por muitos médicos sobre essas doenças ainda é bem limitado. Enfim, na prática, uma vez diante do diagnóstico que você é portador de uma doença que nunca havia ouvido falar a respeito anteriormente, e que ouve do médico, pessoa esta que se imaginava ser a quem poderia lhe ajudar, lhe dizer que a tal doença é rara, que se tem muito pouca informação sobre ela, e que para a mesma não tem cura e nem mesmo tratamento eficaz, e que seu prognóstico é de progressividade, …daí você como parte interessada, o que lhe resta ? … além das buscas na internet por informações, o maior desejo é encontrar outras pessoas que estejam vivendo com o mesmo diagnóstico. O SORRYR-1 tem se prestado a este propósito, tanto que tenho sido procurado por indivíduos afetados e/ou por seus familiares questionando sobre o que tenho feito para lidar com a doença nestes meus 60 anos de vida. Nas primeiras vezes em que fui questionado, confesso que tive dificuldade em responder, primeiro porque entendo que cada pessoa é única, e o que funciona para uma pessoa pode não funcionar para outra, mas com o tempo pude entender que o meu posicionamento pessoal poderia ser algo complementar ao que me propus com o SORRYR-1. Assim sendo, em atendimento a algumas sugestões, decidi escrever de maneira prática sobre o que entendo ser o mais importante para conviver com as doenças relacionadas ao RYR1, e especificamente no meu caso a Miopatia Congênita Centronuclear.
1 - Inicialmente falo sobre minha convicção pessoal dizendo que creio viver esta situação segundo um propósito, me baseando na palavra do apóstolo Paulo em Romanos 12:2 que diz, “.... transformem-se pela renovação da sua mente, para que sejam capazes de experimentar e comprovar a vontade de Deus para sua vida.” , entendendo que apesar das imposições a mim colocada pela doença, busco reinventar e viver um estilo de vida segundo minhas possibilidades, com espírito de resiliência e superação, e busco servir ao próximo como sendo este o propósito de Deus para minha vida.
2 - Atitudes positivas devem ser a palavra de ordem na sua maneira de viver. Assim, entender que o bem-estar emocional é fundamental para uma vida saudável e feliz, faz com que não deixe que sua condição física interfira no seu estado emocional. É importante também lembrar que todos enfrentamos desafios e dificuldades em diferentes aspectos de nossas vidas, e a deficiência física é apenas uma parte de quem somos. Portanto diante do espírito de resiliência e auto-estima positiva, busque se superar nas suas possibilidades e habilidades, não se limitando nas suas limitações, ao contrário, as potencializando.
3 - A atividade física é primordial, é nosso único tratamento disponível, seja fisioterapia ou ginástica, e essa prática deve ser parte de nossa rotina diária. Vale lembrar que nossas células musculares, pela mutação que temos no RYR1 não funciona da maneira correta (contração e relaxamento), interferindo assim em questões relacionadas ao nosso fortalecimento e movimentação, além de poder causar contraturas, rigidez, dores, fadiga, dentre outras. A atividade física, mesmo que passiva, pode nos ajudar com a qualidade de vida e até impedir a progressão da doença. Lançando mão da frase dita por meu neurologista, Dr Acary, que diz, “o RYR1 é movimento”, portanto, movimente, mexa-se, nunca pare de mexer, mexa do músculo do dedo do pé até os da face, assim, mexa-se sempre. Contudo, vale ressaltar que devemos estar atentos ao nosso limite, evitando o excesso de esforço físico e cansaço, pois isso pode agravar os sintomas da miopatia;
4 - O condicionamento respiratório também deve ser um grande ponto de atenção diante das dificuldades musculares generalizadas que enfrentamos. O enfraquecimento da musculatura do tórax, traqueia e diafragma pode interferir em questões sistêmicas. Assim, destaco como exemplo a dificuldade na expectoração de eventuais secreções, deglutição, e adequada troca de gases feita pelos pulmões. Leia mais sobre este tema na postagem “Abordagem Respiratória na Miopatia Centronuclear”;
5 - Outro ponto que deve ser observado é com nosso ganho de peso, uma vez que o quê se ganha nesa situação é a gordura, e como nosso tecido muscular que já não é lá essas coisas, ele é substituído com facilidade pelo tecido gorduroso. O aumento de peso dificulta ainda mais nossa capacidade em fazer atividade física, que por sua vez impede a queima de calorias, favorecendo assim ainda mais o acúmulo de gordura em nosso corpo. Esse acúmulo de gordura em nosso corpo, além de afetar nossa qualidade de vida, pode ainda nos trazer consequências patológicas graves, tais como cardiopatias, diabetes, hipertensão arterial, doenças no fígado, alguns tipos de câncer, problemas renais, dentre outros.
6 - Considerando nossa reduzida capacidade em fazer atividade física, temos uma propensão à fragilidade óssea, portanto, temos que evitar as quedas pelo alto risco de fraturas. Na prática, é que para uma fratura óssea, o tratamento deverá ser desde a imobilização do membro afetado, até a intervenção cirúrgica (observar riscos cirúrgicos), e em ambas situações ficaremos impedidos de movimentação física, o que causará ainda mais perda muscular.
7 - Evite contrair qualquer doença, seja um simples resfriado, ou qualquer outra doença. Por exemplo, nosso corpo diante de uma enfermidade com causa viral ou bacteriana, reage com uma resposta imunológica, liberando uma série de proteínas, as citocinas, as quais produzem uma reação inflamatória não apenas no local da infecção, mas também em outros órgãos, incluindo músculos e articulações, que são nosso maior ponto de atenção e fragilidade. Assim, com esse exemplo procurei mostrar porque uma simples gripe pode nos causar ainda mais fraqueza.
8 - Mantenha um estilo de vida praticando hábitos saudáveis, tais como, seguir uma dieta mais nutritiva, equilibrada, e saudável, ingerindo bastante água (35 ml/kg de peso corporal por dia), procure dormir o suficiente e com qualidade, se exponha periodicamente ao sol (8 às 11 horas), enfim, evite o estresse e preocupação excessiva, assim como hábitos nocivos a saúde física (cigarro, droga, e álcool).
9 - Fique atento e evite tratamentos experimentais, e medicamentos que não os indicados por seu médico especialista. Por exemplo, alguns medicamentos, como estatinas, anti-inflamatórios não esteroides (AINEs), e outros mais, podem piorar a miopatia.
10 - Faça regularmente um acompanhamento médico com especialista visando monitorar não somente sua miopatia, mas também sua condição física geral. É muito importante que os portadores de miopatia conversem com seu médico para discutir os fatores que podem piorar sua condição, e que possam aprender a gerenciá-los.
Foi através do RYR1 Foundation que tive a grande honra e prazer em ter conhecido a Dra Isabelle Marty, PhD, uma cientista que trabalha no INSERM, French National Institute for Medical Reserach. Ela gerencia o C-MyPath (Cellular Myology and Pathology), um centro de pesquisas focado nas doenças neuromusculares, coordenando uma equipe de cientistas, geneticistas, e médicos do Grenoble Institute of Neuroscience na França. Durante meu encontro com a Dra Isabelle, externei a ela sobre nossa ansia como portadores da Miopatia Congênita Centronuclear, uma doença relacionada ao gene RYR1, sobre o aparecimento da cura ou mesmo de um tratamento para a doença, e como contribuição ao SORRYR-1, ela gentilmente enviou um artigo relatando o que está acontecendo nas bancadas de laboratórios de grandes centros de pesquisas científicas ao redor do mundo. O texto reforça meu entendimento de que SER OTIMISTA COM NOSSO FUTURO, É TER FÉ EM DEUS, E ACREDITAR NA CIÊNCIA TRABALHANDO EM NOSSO BENEFICIO.
Segue o texto (tradução por Orlando Carneiro Jr)…
DESENVOLVIMENTO TERAPÊUTICO EM PROGRESSO PARA MIOPATIAS RELACIONADAS AO RYR1
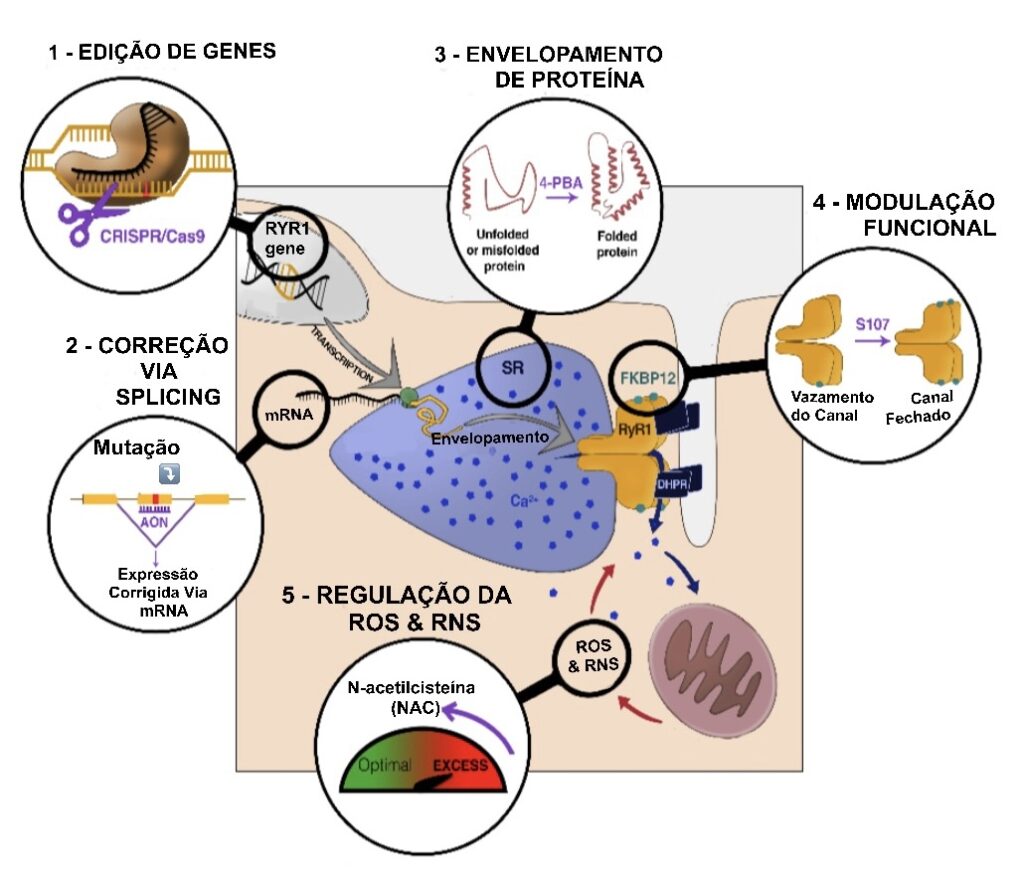
Ainda não existe nenhum tratamento para as miopatias relacionadas ao gene RYR1, em parte devido ao número de mutações, mas também pela diversidade de suas consequências. Um pré-requisito para o desenvolvimento terapêutico para a doença é a disponibilidade de modelos de pesquisa (cobaias) que reproduzam as características da doença, assim como ter uma boa compreensão dos mecanismos fisiopatológicos (funcionamento da doença). Contudo, esses dois aspectos estão em rápida evolução, pois muitos modelos celulares ou animais (cobaias) foram desenvolvidos recentemente, e diferentes abordagens estão sendo avaliadas, seja em pesquisas básicas, em estudos pré-clínicos, ou mesmo em ensaios clínicos (clinical trials). Estes estudos podem ser classificados como “estratégias gerais”, tendo como alvo o mecanismo fisiopatológico normalmente verificado em diferentes mutações/pacientes, tais como moléculas químicas, ou “estratégia orientada personalizada ao paciente”, tendo alvo a mutação específica de cada paciente, como exemplo a terapia gênica.
As abordagens farmacológicas visam testar moléculas que interagem com gene RYR1 ou com suas proteínas associadas, visando sempre na busca de melhorar a função do canal ou as vias fisiológicas do RYR1. Por outro lado, a terapia gênica foca diretamente o gene mutado ou via mRNA para corrigir a própria proteína do RYR1, restaurando assim a expressão funcional da proteína. Em ambas as abordagens, o objetivo é restaurar a homeostase normal do cálcio e, posteriormente, a força muscular.
ABORDAGENS FARMACOLÓGICAS
O uso de compostos químicos para corrigir as alterações funcionais do gene RYR1 baseia-se na decifração precisa dos mecanismos fisiopatológicos e na identificação de moléculas que atuam no mecanismo alvo, geralmente capazes de restaurar a homeostase do cálcio. Esses compostos podem atuar diretamente no RYR1, alterando suas propriedades, conformação e/ou interação com proteínas reguladoras, a fim de restaurar o fluxo normal de cálcio, mas também de agir nas consequências causadas pela alteração do curso do fluxo de cálcio. Cada mutação pode resultar em diferentes mecanismos fisiopatológicos, por isso é importante identificar diferentes famílias de moléculas, para os diferentes mecanismos. Outro aspecto importante é o uso prévio ou já utilização de compostos químicos para humanos, o que poderia reduzir drasticamente o atraso entre a prova de conceito da eficácia e seu lançamento à comercialização.
Em se tratando de estudo dos mecanismos fisiopatológicos, a primeira alteração celular identificada é um elevado estresse oxidativo, observado em muitos modelos portadores de miopatias relacionadas ao RYR1, de zebrafish a camundongos, e em cultura muscular primária em pacientes. Seguindo essa linha, foi testado com sucesso nesses diferentes modelos, o tratamento com o antioxidante N-Acetilcisteína (NAC) resultando na melhora de suas características moleculares e fisiológicas. Esses resultados encorajadores observados nos referidos modelos, levaram pesquisadores a promover ensaios clínicos a fim de testar a eficácia do NAC para diminuir o elevado estresse oxidativo, assim como aumentar a resistência física em pacientes com miopatias relacionadas ao RYR1. Esse estudo com NAC confirmou o aumento do estresse oxidativo nos pacientes portadores de doenças relacionadas ao RYR1, mas o tratamento não foi capaz de corrigir esse aumento em comparação ao grupo placebo. Do ponto de vista funcional, o resultado embora tenha sido medido um ligeiro aumento na distância percorrida (6MWT - six minute walk test ), não atingiu valores com significância.
O segundo mecanismo alterado com algumas mutações é a interação do RYR1 com sua proteína de ligação, ou proteína reguladora FKBP12 (também chamada calstabina), a qual visa manter o canal de cálcio do RYR1 eficientemente fechado. A consequência dessa alteração é um vazamento do cálcio contido nas reservas de cálcio do músculo, fazendo com que a estimulação do músculo não levará a uma liberação de cálcio suficiente para produzir uma contração normal. Pesquisadores identificaram moléculas denominadas RyCals, capazes de reduzir esse vazamento de cálcio, trazendo assim a abordagens terapêuticas promissoras. Testes clínicos foram lançados pela ARMGO Pharma Inc, em um número restrito de pacientes que apresentaram um “RYR1 com vazamento" confirmado, fornecendo resultados encorajadores sobre tolerância e dor muscular. O benefício agora deve ser confirmado no nível de força muscular em um grupo maior de pacientes.
As proteínas são classes de macromoléculas biológicas de maior importância no metabolismo celular e na fisiologia dos organismos, e alguns mecanismos celular naturais, como o enovelamento de proteínas (protein folding), também mostraram ser alterados, o que faz com que a célula não desempenhe sua função correta, e o tratamento de alguns modelos de camundongos com 4-fenilbutirato de sódio (4-PBA), droga que melhora o enovelamento de proteínas, mostrou algum benefício no animal, mas ainda não foi testado em humanos.
Muitas equipes de pesquisadores ao redor do mundo estão trabalhando para identificar moléculas que possam melhorar a liberação de cálcio muscular, seja no reposicionamento de moléculas usadas para outras condições (drogas já utilizadas para outras doenças), ou para identificar novas moléculas que nunca foram testadas em animais ou humanos (nova droga).
TERAPIA DE GENES
Uma vez identificada a mutação responsável por uma doença, o objetivo das abordagens de terapia gênica é modificar o genoma das células do indivíduo afetado para corrigir essa mutação e restaurar de forma sustentável a função alterada caracterizada na patologia. Uma questão importante para as doenças neuromusculares é a capacidade de atingir todos os músculos do corpo e especialmente os músculos respiratórios (diafragma e músculos intercostais) que estão entre os menos acessíveis à injeção. Existem várias maneiras de desenvolver uma estratégia gênica, dependendo da mutação alvo, sua localização na sequência de DNA, e suas consequências na função proteica.
A substituição gênica, é a introdução de uma cópia nova e funcional de um gene alterado através de um vetor viral, estratégia considerada interessante para as mutações de perda de função. O uso de um vetor viral como o Vírus Adeno-Associado (AAV) permite com uma única injeção intravenosa, atingir todos os músculos do corpo, mesmo os músculos respiratórios e diafragma menos acessíveis. Um resultado espetacular da terapia genética foi obtido para Atrofia Muscular Espinhal (AME). Esta promissora abordagem terapêutica tem, infelizmente, algumas limitações, relacionadas com a capacidade de empacotamento do vetor viral utilizado. Atualmente, não é possível integrar a sequência de codificação do RYR1, que é muito grande, nem é possível integrar uma versão truncada mais curta e funcional do RYR1.
Quando a correção no gene é muito complexa, como por exemplo nos genes grandes, uma estratégia alternativa é direcionar o mRNA, chamado de RNA mensageiro, que funciona carregando a informação entre o gene e a proteína. A correção do RYR1 via mRNA é especificamente adequada para um subgrupo de mutações, no caso, as mutações que resultam na presença de um segmento adicional na proteína (o chamado "exon"), para o qual a estratégia "exon skipping" que não modifica o gene que possui a mutação, mas ele interfere e modifica o processo de transferência da informação genética e, portanto, as instruções ou mecanismos de funcionamento do RYR1. Esta abordagem tem mostrado resultados extremamente encorajadores e está em desenvolvimento clínico para algumas doenças neuromusculares entre as quais Distrofia Muscular de Duchenne (DMD) e Atrofia Muscular Espinhal (SMA - Spinal Muscular Atrophy).
Um novo campo de trabalho surgiu recentemente e está crescendo exponencialmente, que é a correção gênica por CRISPR/Cas9. A base deste sistema de edição de genes, também chamado de “tesoura molecular”, é separar o DNA em um local muito específico e escolhido, a fim de deletar uma parte do DNA (por exemplo a que contém a mutação) e assim substituí-la por um novo DNA ( sem a mutação). Até agora, para doenças musculares em modelos animais, só era possível deletar um segmento de DNA mutado, mas não substituí-lo. Mas o avanço tecnológico está evoluindo em uma velocidade impressionante e novas ferramentas de edição de genes estão sendo desenvolvidas, capazes teoricamente de corrigir qualquer mutação, pelo menos em modelos celulares, como por exemplo o Prime-editing, ferramenta mais complexa que a edição CRISPR/Cas9, porque ela pode excluir comprimentos longos de DNA causador de doença ou mesmo inserir DNA para reparar mutações.
A terapia gênica é um novo desafio para doenças genéticas, a qual era apenas um sonho há 20 ou 30 anos atrás. Apesar de todos os desafios que a abordagem de edição genética está enfrentando, soluções devem ser encontradas antes de passar para um tratamento real em humanos, além de uma série de questões éticas que foram levantadas por esta nova tecnologia, a terapia gênica e edição de genoma parecem ter o maior potencial terapêutico a longo prazo.
 CONCLUSÃO
CONCLUSÃO
Embora nenhum tratamento esteja disponível para as doenças relacionadas ao RYR1, as vias terapêuticas estão sendo exploradas ativamente. Da terapia farmacológica mais antiga, usada há muito tempo, com efeitos colaterais conhecidos e benefícios mais ou menos modestos, à mais nova terapia genética com efeitos colaterais desconhecidos e enormes benefícios potenciais esperados, a terapia intermediária perfeita ainda precisa ser descoberta. Ou seja, uma combinação de diferentes abordagens pode ser uma boa alternativa, como um composto químico capaz de reduzir a quantidade de vetor viral necessária para terapia gênica, melhorando a entrada no músculo, ou melhorando a estrutura muscular. Embora os sucessos recentes em diferentes doenças neuromusculares provavelmente tenham gerado novas esperanças, a pesquisa ativa deve continuar nas duas direções, pois ainda é difícil prever hoje qual será o futuro das terapias para as doenças relacionadas ao RYR1, sendo as terapias de curto e longo prazo provavelmente a milhas de distância.
RABDOMIÓLISE EXERCICIONAL RELACIONADA AO RYR1, DOENÇA COMUM, MAS PROVAVELMENTE UMA DISFUNÇÃO DO RECEPTOR DE RIANODINA DO MÚSCULO (RYR1) SUBDIAGNOSTICADA
Rabdomiólise é uma doença caracterizada pela destruição das fibras musculares, ou seja, é a quebra do tecido muscular que leva à liberação do conteúdo das fibras musculares no sangue. A rabdomiólise é caracterizada por uma tríade de mialgia, fraqueza muscular e escurecimento da urina. Esta combinação particular de sintomas está presente em uma minoria de indivíduos. A característica é uma creatinina quinase fortemente elevada, superior a dez vezes o limite máximo. As causas mais comuns da Rabdomiólise são abuso de substâncias, medicação e trauma.
Mutações no gene do receptor de rianodina do músculo esquelético (RYR1) estão associadas a um amplo espectro de miopatias hereditárias que se apresentam ao longo da vida. A Suscetibilidade à Hipertermia Maligna (SHM) relacionadas à mutações no RYR1 tem surgido como uma causa comum de Rabdomiólise Exercicional, representando até 30% dos episódios de rabdomiólise em indivíduos saudáveis. A maioria dos indivíduos são normalmente fortes, e não têm história pessoal ou familiar de Hipertermia Maligna.
A explicação sobre o desenvolvimento da Rabdomiólise Exercicional se dá por uma falha do mecanismo de regulação da temperatura do corpo quando exposto a temperaturas excessivamente altas, podendo ser causado pelo desequilíbrio entre (1) fatores ambientais (gatilhos) e (2) predisposição (suscetibilidade). Se o indivíduo for exposto a múltiplos gatilhos, mesmo aqueles sem suscetibilidade aumentada, também podem desenvolver um episódio de rabdomiólise. Ao mesmo tempo, indivíduos com predisposição genética (suscetibilidade) à rabdomiólise poderão desenvolver um episódio da doença se não forem expostas a gatilhos suficientes.
Os gatilhos, ou fatores ambientais (1) que podem levar à Rabdomiólise Exercicional são: esforço físico excessivo (além do limiar de dor muscular/esforço físico e/ou muito mais do que seria apropriado no nível de treinamento no momento); um forte desejo ou compulsão para completar o esforço (por exemplo, em competições ou em treinamento militar); exercício quando ainda há muita dor muscular proveniente de treinamento anterior; contrações musculares excêntricas (exercícios em que o músculo se alonga durante a contração); desidratação antes, durante ou após o exercício; jejum antes do exercício; exercício em ambientes quentes;, esportes em ambiente úmido ou com roupas muito quentes (que impeçam suficientemente o calor de sair do corpo, com risco de insolação); certos medicamentos; esportes durante um episódio de gripe/infecção por uma outra forma de vírus (possivelmente com o uso de anti-inflamatórios não esteróides); e excesso de álcool, cafeína, ou outras drogas, e doping antes, ou após esforço físico.
Com relação à predisposição ou suscetibilidade (2), em alguns casos de Rabdomiólise uma causa hereditária deve ser levada em consideração, por exemplo, em episódios recorrentes da doença muito grave, em que o nível de CK permanecer elevado por muito tempo mesmo após um episódio; se não houver sinais de causas externas aparentes, ou se houver queixas na família ou histórico familiar que correspondam a uma doença muscular. Já se sabe que mutações no gene RYR1 estão associados a até 30% dos episódios de Rabdomiólise Exercicional. Sabe-se também sobre a existência de uma correlação entre a Hipertermia Maligna e a Rabdomiólise Exercicional, porém ainda em estudo. Daí nestes casos a necessidade de uma pesquisa por um diagnóstico conclusivo, feitos por exames adicionais, que podem ser através de ultrassonografia muscular, biópsia muscular, e pesquisa genética.
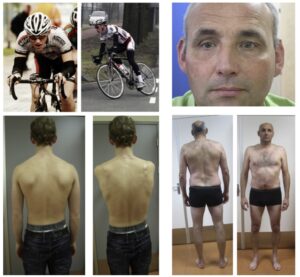
Na imagem um ciclista semi-profissional de 17 anos com histórico de episódios de Rabdomiólise de Exercicional (ERM) recorrente relacionada ao RYR1. Observe a fraqueza leve na musculatura axial. Um tio paterno portador da mesma mutação genética que apresentou no passado mialgia por esforço, também pode-se verificar no exame como tendo uma constituição muscular e ptose unilateral leve, característica de portadores da mutação genética.
Complicações - A principal complicação da Rabdomiólise Exercicional é a insuficiência renal aguda devido à obstrução tubular pela mioglobina liberada no sangue. Por causa da mioglobinúria, a urinálise será positiva para hemoglobina, mas não há eritrócitos microscópicamente visíveis. A insuficiência renal aguda ocorre em 14 a 46% dos pacientes. Outras complicações incluem síndrome compartimental, hipercalemia, hipocalcemia e insuficiência hepática. A mortalidade por rabdomiólise é de cerca de 10% dos casos.
Mecanismo de Funcionamento - Com base em estudos em modelo (camundongos), em testes de esforço/estresse por calor ambiental e miopatia, a possível fisiopatologia (funções fisiológicas da doença) da Rabdomiólise relacionada a mutações no RYR1 relacionadas a MHS (Susceptibilidade à Hipertermia Maligna), mostra que (1) os canais RYR1 são mais sensíveis e suscetíveis a eventuais ativação elétrica pelos ións de Ca, causando um vazamento de Ca2+; (2) o aumento dos níveis de [Ca2+] no citoplasma estimula a produção de Espécies Reativas de Nitrogênio; e (3) subsequente aumento da S-Nitrosilação, que; (4) por sua vez aumenta a sensibilidade à temperatura. A S-nitrosilação também diminui a sensibilidade do RYR1 à inibição do Ca2+, promovendo ainda mais o vazamento de Ca2+, isso resulta em (5) adicionais aumentos de Ca2+, e aumenta ainda mais a produção de ROS/RNS (Espécies Reativas do Oxigênio/Espécies Reativas de Nitrogênio), levando a um mecanismo de ciclo vicioso de alimentação. Finalmente, níveis cronicamente elevados de Ca2+ e ROS/RNS (Espécies Reativas do Oxigênio/Espécies Reativas de Nitrogênio) danificam as mitocôndrias e contribuem para o desenvolvimento de miopatia. Em caso de estresse por calor (6) devido ao exercício em ambientes quentes, a liberação de Ca2+ pelos receptores RYR1 mutados é grande e persistentemente aumentada, eventualmente levando à insolação. Além disso, infecções virais e drogas médicas e/ou recreativas podem reforçar também os riscos e mecanismo do ciclo de alimentação da doença. Verifique o esquema a seguir...

O texto acima foi gentilmente cedido por Dr Nicol Voermans, MD, PhD, que trabalha no Radboud University Medical Center (Holanda) com pesquisas sobre miopatias hereditárias raras. Dr Nicol, além de ter sido co-diretora do Workshop Internacional de Pesquisas em Doenças Relacionadas ao RYR1 realizado em Julho de 2022 em Pittsburgh, E.U., contribuiu com uma brilhante palestra sobre doenças relacionadas ao RYR1 na idade adulta, no caso da Hipertermia Maligna e Rabdomiólise Exercicional.
Vale destacar que o referido texto foi originalmente escrito em holandes (dutch), traduzido para o inglês, e aqui neste site, traduzido para o protuguês e contextualizado para o leitor do SORRYR-1.
ESPERANÇA AOS PORTADORES DE DOENÇAS RELACIONADAS AO RYR1 VISTA POR UM OUTRO LADO DO PRISMA
Na postagem anterior tratei sobre as boas notícias que tive durante o workshop científico sobre as doenças relacionadas ao RYR1 em Pittsburgh (EUA), em julho de 2022. Me referi às pesquisas sobre uma droga capaz de aliviar, tratar, e até curar as doenças relacionadas ao RYR1, mencionei inclusive sobre valores de investimentos em pesquisas e tendências de mercado para os próximos anos. Contudo pode ter ficado uma pergunta no ar, sobre o porquê do grande interesse em pesquisas tão dispendiosas sobre uma doença que atinge um pequeno número de pessoas. …então vamos buscar o raciocínio lógico…
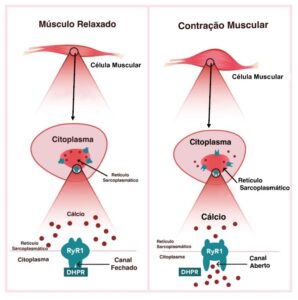
Músculo é o tecido responsável pelo movimento do corpo humano. O mecanismo de funcionamento do músculo, ou seja, como ele contrai e relaxa, é chamado de acoplamento excitação-contração (EC), e tudo acontece na célula da fibra muscular, onde o citoplasma está localizado. Lá dentro, o Retículo Sarcoplasmático (RS) atua como reservatório para íons de cálcio, essenciais para desenvolver a força muscular. O receptor de Ryanodina Tipo 1 (RYR1) funciona como canal liberador dos íons de cálcio, o qual quando liberado no citoplasma, faz com que o músculo se contraia. Na prática o mecanismo de funcionamento é simples, quanto mais íons de cálcio liberado no citoplasma, mais força muscular o indivíduo desenvolve.
O cientista Andrew R. Marks, MD, professor de fisiologia e biofísica celular na Universidade de Columbia (EUA), explica em seus estudos que a perda da função muscular é associada à disfunção dos canais de liberação do receptor de rianodina (RYR1) do músculo, e que pode ser causado por uma falha decorrente a uma mutação genética, ou devido à sobrecarga oxidativa celular relacionada à idade. Essa falha desestabiliza o estado fechado do canal, resultando em um defeito pelo vazamento de cálcio intracelular, acarretando em função muscular reduzida, o que explica não somente as doenças relacionadas ao RYR1, mas também explica no caso da oxidação celular, a razão pela qual os exercícios físicos se tornam mais difíceis com a idade.
A boa notícia é que existe uma droga em fase de testes que pode barrar esse vazamento. Na pesquisa foram estudadas as células musculares de ratos novos e velhos. Um rato de seis meses cujos receptores de rianodina vazavam cálcio mostraram os mesmos problemas de fraqueza muscular do que um rato mais velho. Este, por sua vez, apresentou melhoras depois de ser tratado com a droga em teste. O estudo sugere aos cientistas procurarem por novos caminhos no tratamento do envelhecimento. “As pesquisas que temos visto se focam em produzir mais músculos”, diz Andrew Marks. “E a diferença é que nós focamos não no músculo, mas no seu mecanismo de funcionamento, pois o aumento de músculos não ajuda se eles não funcionarem.”
Portanto, entendo que quando a comunidade científica desenvolve pesquisas em busca de uma droga capaz de tratar e até curar as doenças musculares relacionadas ao RYR1, se busca também beneficiar todos os indivíduos, porque a fraqueza muscular decorrente do envelhecimento é comum a todos. Assim, podemos pensar que o interesse mercadológico para a descoberta de uma droga capaz de atuar no defeito ou mal funcionamento da célula muscular, pode ser maior por ir de encontro com a necessidade de todos os indivíduos, e não somente aos portadores de doenças relacionadas ao RYR1. Por fim eu faço a seguinte analogia, nós portadores de uma doença relacionada ao RYR1 temos um defeito de fábrica, que é a mutação genética, e os indivíduos saudáveis terão um defeito por conta do tempo ou idade, que é a oxidação celular.
O WORKSHOP COM PESQUISADORES DE 8 PAISES DIFERENTES QUE ACONTECEU DURANTE A CONFERÊNCIA INTERNACIONAL SOBRE DOENÇAS REALCIONADAS AO RYR-1 REALIZADA EM JULHO DE 2022 EM PITTSBURGH, EUA, TROUXE GRANDES NOVIDADES SOBRE PESQUISAS EM BUSCA DE TRATAMENTO E CURA DA DOENÇA
A descoberta de qualquer doença, nunca é algo esperado, é bem desagradavel, e no caso de uma doença grave será sempre uma novidade traumática. Acontece que na grande maioria das doenças existe a opção ao afetado de um tratamento que funciona como um alento e até motivação para o novo momento que será vivido até que se alcance sua cura. Contudo, existem aquelas doenças com prognóstico evolutivo, que não contam com tratamento, muito menos cura, e que fazem com que só reste ao afetado ter que encarar a realidade do diagnóstico, e desenvolver por si só meios para conviver com suas dificuldades, sejam as físicas e as emocionais.
Recentemente participei da Conferência Internacional sobre as Doenças Relacionadas ao RYR-1, que contou com a presença de mais de 200 pessoas entre afetados e familiares, evento este que foi precedido por um workshop que reuniu 45 pesquisadores presenciais e 10 virtuais de 8 países diferentes, os quais compartilharam seus trabalhos em busca de tratamento ou cura da doença. O evento além de promover a sociabilização entre os participantes, teve como objetivo, através dos palestrantes, informar questões conceituais sobre a doença, até às novidades sobre as pesquisas para tratamentos da doença.
Como as doenças relacionadas ao RYR1 ainda não contam com tratamento, muito menos cura, foi natural observar a grande ansiedade entre os presentes em saber sobre as novidades do andamento das pesquisas em busca de uma droga capaz de aliviar sintomas e tratar as complicações causadas pela doença.
Providencialmente os cientistas palestrantes foram portadores de boas notícias que vieram de encontro com o anseio dos presentes, e informaram que estão trabalhando ativamente por meio de várias abordagens de pesquisas em busca por uma droga capaz de aliviar os sintomas da doença, contudo este é um processo bem complexo, e normalmente leva muitos anos e altos custos de investimentos.
Falando em alto custo, algo que parecia tão distante, mas que já faz parte de nossa realidade, foi pessoalmente abordado por Jacques Tremblay, PhD, cientista responsável da University of Laval, Québec, Canadá, pelas pesquisas da terapia de reposição gênica através da correção da mutação pontual no gene RYR1 usando a tecnologia de edição CRISPR/Prime editing technology. Com a “edição de genes”, o objetivo é corrigir ou “editar” apenas uma pequena parte do gene “defeituoso”, oferecendo assim o potencial de cura para doença, não apenas um tratamento.
pessoalmente abordado por Jacques Tremblay, PhD, cientista responsável da University of Laval, Québec, Canadá, pelas pesquisas da terapia de reposição gênica através da correção da mutação pontual no gene RYR1 usando a tecnologia de edição CRISPR/Prime editing technology. Com a “edição de genes”, o objetivo é corrigir ou “editar” apenas uma pequena parte do gene “defeituoso”, oferecendo assim o potencial de cura para doença, não apenas um tratamento.
Várias pesquisas de medicamentos estão em desenvolvimento como terapias potenciais para as doenças relacionadas ao RYR1 (DR-RYR1). Para mim a grande novidade foi saber que alguns desses medicamentos já estão aprovados para outras doenças, e os pesquisadores estão testando o “reposicionamento dessas drogas” para as doenças relacionadas ao RYR1 (DR-RYR1), como por exemplo, MitoQ, Dantroleno, Ácidos Graxos Poli-insaturados, Salbutamol, Piridostigmina, NAC (N-Acetil L-Cisteína), dentre outros.  Algumas destas drogas têm como alvo o próprio receptor RYR1, outras visam características e sintomas específicos das DR-RYR1. O reposicionamento de fármacos (medicamentos) consiste na técnica de pesquisa e identificação de novas indicações terapêuticas além dos já conhecidos. O seu desenvolvimento clínico requer menos tempo e menos etapas, visto que o perfil de segurança do medicamento já é conhecido, demonstrado e aprovado, assim como por ter um investimento mais baixo. A pesquisa de novas indicações terapêuticas pressupõe abordagens experimentais e computacionais que busquem identificar e gerar novas hipóteses de interações fármaco-alvo desconhecidas até então. Exemplos conhecidos de reposicionamento de fármacos é o Viagra, que foi inicialmente desenvolvido para tratar hipertensão e angina, mas que durante as etapas de estudo clínico acabou sendo direcionado para tratar disfunção sexual masculina, e outro famoso foi o caso da Zidovudina (AZT), primeiro fármaco aprovado para tratamento da AIDS, e cuja indicação original era o câncer.
Algumas destas drogas têm como alvo o próprio receptor RYR1, outras visam características e sintomas específicos das DR-RYR1. O reposicionamento de fármacos (medicamentos) consiste na técnica de pesquisa e identificação de novas indicações terapêuticas além dos já conhecidos. O seu desenvolvimento clínico requer menos tempo e menos etapas, visto que o perfil de segurança do medicamento já é conhecido, demonstrado e aprovado, assim como por ter um investimento mais baixo. A pesquisa de novas indicações terapêuticas pressupõe abordagens experimentais e computacionais que busquem identificar e gerar novas hipóteses de interações fármaco-alvo desconhecidas até então. Exemplos conhecidos de reposicionamento de fármacos é o Viagra, que foi inicialmente desenvolvido para tratar hipertensão e angina, mas que durante as etapas de estudo clínico acabou sendo direcionado para tratar disfunção sexual masculina, e outro famoso foi o caso da Zidovudina (AZT), primeiro fármaco aprovado para tratamento da AIDS, e cuja indicação original era o câncer.
Outra grande novidade foi saber sobre o RYCALS, que é uma nova classe de medicamentos que atua diretamente no receptor RYR1, estabilizando e melhorando a ligação de RYR1 e calstabina, restaurando assim a vedação para evitar vazamento de cálcio, situação essencial para o bom funcionamento da célula muscular. Pesquisadores mostraram que o tratamento com RYCALS restaura a função muscular em camundongos in vivo e no tecido muscular humano ex vivo. Especificamente, um estudo recente mostrou que RYCALS melhorou a ligação da calstabina a o receptor RYR1 em células musculares retiradas de biópsias de pacientes com doenças relacionadas ao RYR1. No final do ano de 2021, a ARMGO Pharma, desenvolvedora do RYCALS, recebeu um investimento de US$ 35 milhões de uma empresa europeia de capital de risco. Um teste clínico humano de Rycals foi concluído . O Dr. Payam Mohassel, membro da Fundação RYR-1 e investigador principal do estudo RYCALS, fez uma apresentação muito antecipada na Conferência da Família que resumiu as principais descobertas deste importante estudo. Especificamente, o estudo revelou que o RYCALS foI bem tolerado pelos pacientes sem efeitos colaterais. Embora o estudo tenha sido pequeno, demonstrou algumas tendências promissoras em testes que mediram os sintomas de fraqueza e fadiga dos pacientes. Diante dessas descobertas, o Dr. Mohassel e a equipe de desenvolvimento clínico do RYCALS acreditam que o desenvolvimento clínico adicional da droga é garantida.
Por fim, eu fico muito animado por saber que, corroborando com o relato acima descrito, de acordo com informações obtidas da Data Bridge Market Research , empresa de análise de mercado, espera-se que o mercado de pesquisas farmacêutico de doenças relacionadas ao receptor de rianodina tipo 1 (RYR1) cresça 6,40% a uma taxa anual composta (CAGR) no período de previsão de 2021-2028.
A FUNDAÇÃO RYR-1 REALIZOU EM JULHO DE 2022, EM PITTSBUGH, EUA, O PRIMEIRO WORKSHOP INTERNACIONAL DE PESQUISAS SOBRE DOENÇAS RELACIONADAS AO RYR-1
A Fundação RYR-1 realizou nos dias 21 e 22 de julho último, em Pittsburgh, nos Estados Unidos, o primeiro Workshop Internacional de Pesquisas sobre Doenças Relacionadas ao RYR-1, para discutir desde os mecanismos ao tratamento da doença. O evento reuniu 45 pesquisadores presenciais e 10 virtuais de 11 países diferentes, os quais se encontram desenvolvendo trabalhos em busca de tratamento ou cura da doença, e que na oportunidade puderam compartilhar entre eles suas respectivas pesquisas.
A organização do encontro convidou também 10 indivíduos afetados pelas doenças relacionadas ao RYR1, estando eu entre eles, para relatar nossas diferentes histórias de vida em relação à doença. O objetivo foi compartilhar nossa vivência, conhecimentos e interagir com os presentes, visando assim colaborar no desenvolvimento de novas estratégias para encontrar terapias, assim como também sensibilizar os pesquisadores sobre nosso anseio urgente por alguma forma de resultado prático de suas pesquisas para amenizar sintomas e até curar a doença.
No meu testemunho de vida diante da doença, em que relatei acontecimentos desde meu nascimento até os dias de hoje, teve três pontos que percebi chamar a atenção dos presentes. Um dos pontos foi sobre a exaustão sofrida em função do longo período de 44 anos que se levou para o diagnóstico. Essa mesma demora de tempo para diagnostico não seria uma realidade nos dias de hoje, mas ainda deve ser considerada como alta, pois sabe-se que atualmente uma “doença rara” leva em média de 7 a 10 anos para ser diagnosticada. No meu caso, a Miopatia Congênita Centronuclear não é uma das doenças mais comuns dentro do espectro das relacionadas a mutação do RYR-1, dificultando assim o seu diagnóstico. Outro ponto importante destacado foi dizer que mesmo recebendo o diagnóstico da doença, a falta de informação dado ao seu pouco conhecimento médico-científico, me causou o que disse ter sido uma espécie de cura emocional, gerando um grande estímulo positivo em busca de respostas ao desconhecido da doença. Entendo que a falta de diagnóstico e informações sobre uma doença, muitas vezes é pior do que seus próprios sintomas, e que o emocional tem um grande poder sobre o físico. E por fim, disse sobre o grande  momento vivido depois de 10 anos do diagnóstico, em que conheci a Fundação RYR-1, momento aquele em que ainda buscava informação sobre a doença. Essa organização tem o objetivo promover a troca de experiências entre os participantes, além de apoiar cientistas que trabalham no desenvolvimento de medicamentos e tratamento, a qual mostrou a mim que a Miopatia Congênita Centronuclear não era um campo tão desconhecido como pensava, e me fez acreditar em algo que eu nunca tinha pensado antes, que era a existência próxima de um medicamento para tratar ou aliviar os efeitos das Doenças relacionadas ao RYR1.
momento vivido depois de 10 anos do diagnóstico, em que conheci a Fundação RYR-1, momento aquele em que ainda buscava informação sobre a doença. Essa organização tem o objetivo promover a troca de experiências entre os participantes, além de apoiar cientistas que trabalham no desenvolvimento de medicamentos e tratamento, a qual mostrou a mim que a Miopatia Congênita Centronuclear não era um campo tão desconhecido como pensava, e me fez acreditar em algo que eu nunca tinha pensado antes, que era a existência próxima de um medicamento para tratar ou aliviar os efeitos das Doenças relacionadas ao RYR1.
Encontros como as conferências de famílias, e esse primeiro workshop de pesquisadores, me fazem entender que apesar de raro ou em meio a poucos, não me encontro sozinho, e assim além de aprender com os outros sobre como conviver com a doença, alimenta a expectativa em saber que existem médicos e cientistas em adiantado estágio de pesquisa por uma droga para tratamento e até a sua cura.